Service
服務項目

臨床研究執行
01. 專案管理
02. 試驗啟動管理
03. 試驗機構管理
04. 執行經驗
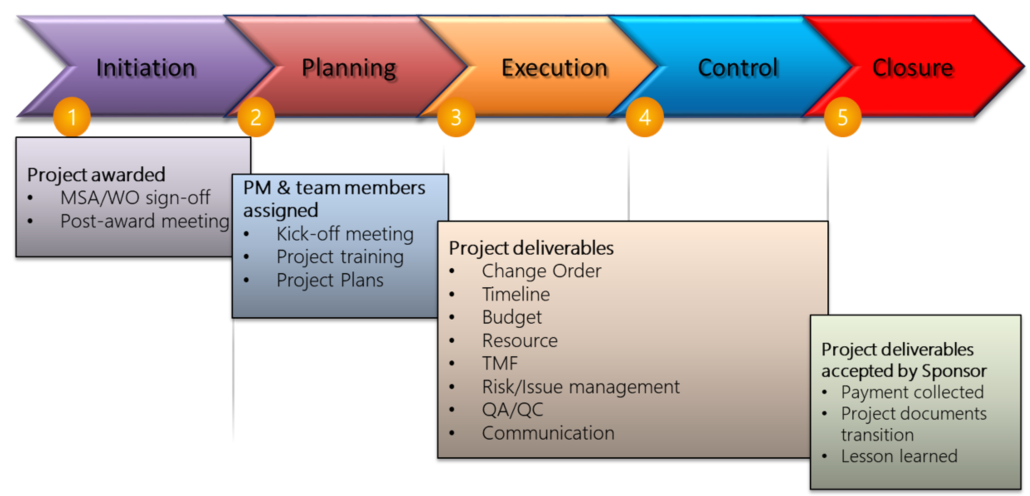
01. 專案管理
我們的專案管理團隊來自國內外藥廠或CRO工作經驗,並具備超過10年以上的國內外專案計畫執行經驗與專業知識,有效運用臨床試驗管理系統(CTMS)追蹤專案執行進度、財會系統控管預算與支出、電子檔案管理系統偵測文件完整度,並依標準作業流程嚴格執行計畫以確保試驗品質。我們的經營理念是做最友善的CRO,提供客製化的客戶需求。
02. 試驗啟動管理
引用臨床試驗管理系統(CTMS)篩選潛在研究中心和研究者資料庫;目前已建構與國內超過30家試驗機構合作的經驗。配合衛福部食藥署(TFDA)全面使用藥品查驗登記審查暨線上申請作業平台(ExPRESS)進行IND電子提交申請以提升審查效率,並且運用電子公文交換系統及時取得回覆或核准,節省紙本公文旅行時間。
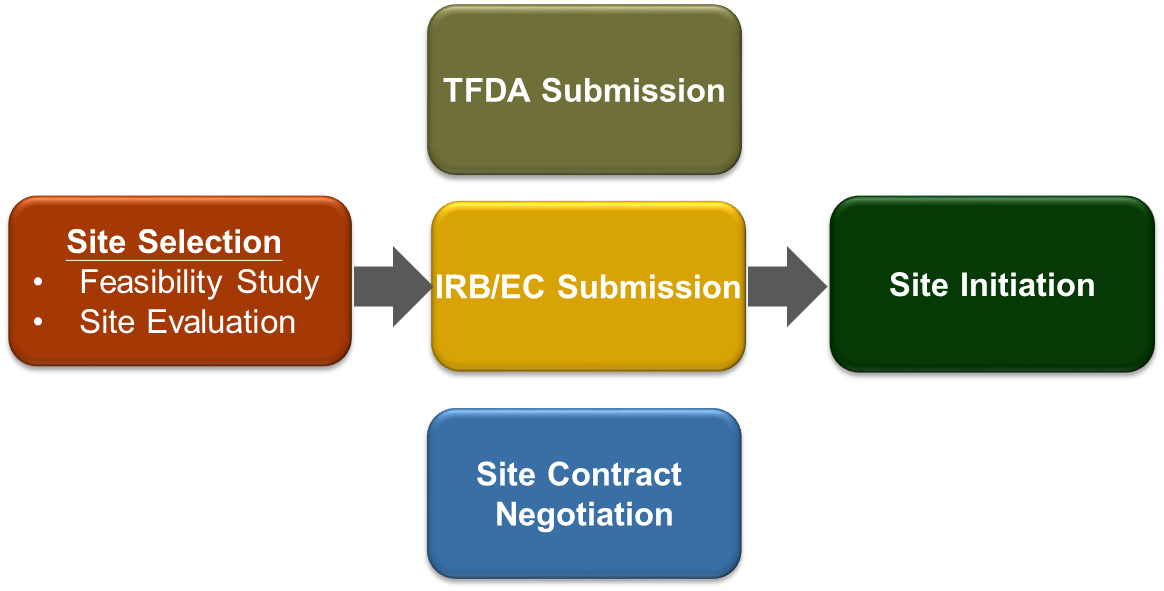
- 試驗機構篩選 - 可行性評估及試驗機構實際訪查
- 送審文件撰寫與準備
- 監管機構送審提交
- 人體試驗委員會送審提交
- 試驗機構合約擬定與談判
- CDE臨床試驗資訊網每半年更新一次
03. 試驗機構管理
應用臨床試驗管理系統(CTMS)監控專案進度、完成監測報告、追蹤試驗偏差和SAE通報,以及(電子)試驗檔案(eTMF)管理。為了保持研究品質,定期執行EDC和CTMS之間的計畫偏差一致性檢查。
- 試驗機構啟動
- 試驗機構定期監測訪視
- 協助試驗機構相關事務管理
- 受試者收納計畫、策略與推動
- 提供試驗更新後核心文件之教育訓練
- 支付試驗機構款項之計算與管理
- 試驗機構之共同監測訪視
- 試驗機構之試驗結束訪視
- 試驗文件管理系統 (使用DIA 3.2.0最新版本架構)
04. 執行經驗
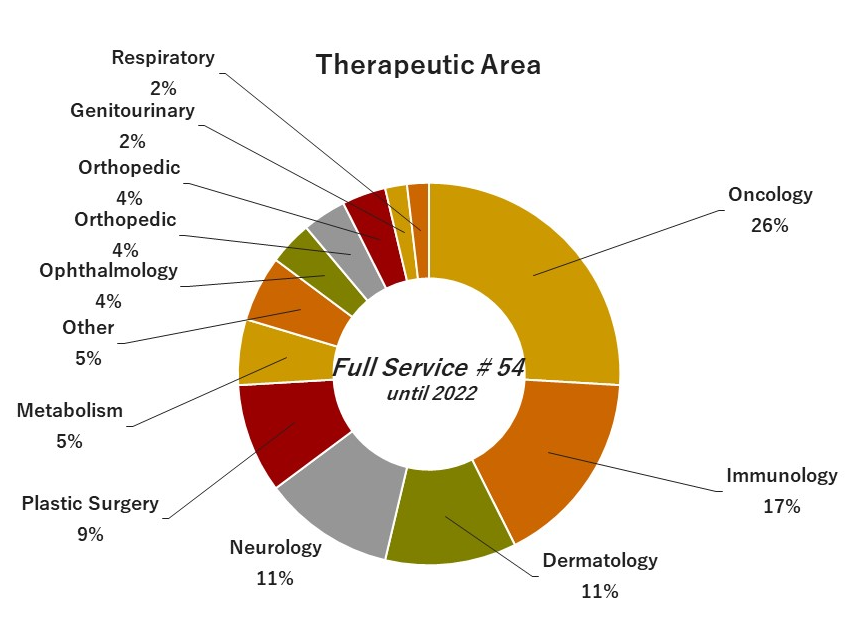 |
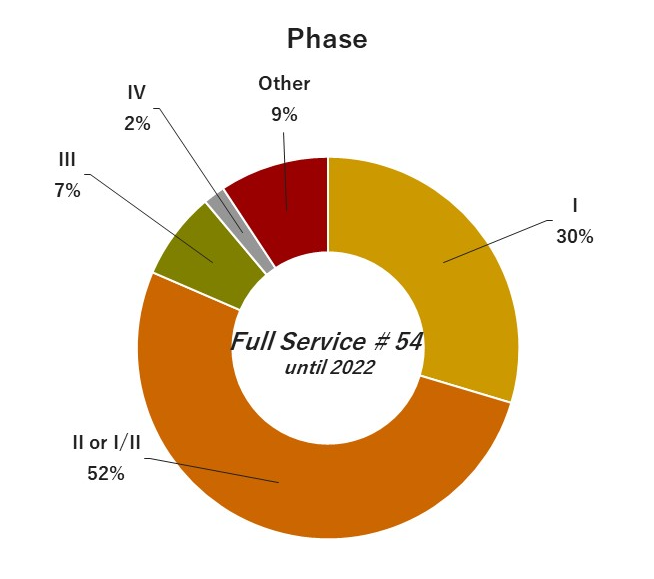 |
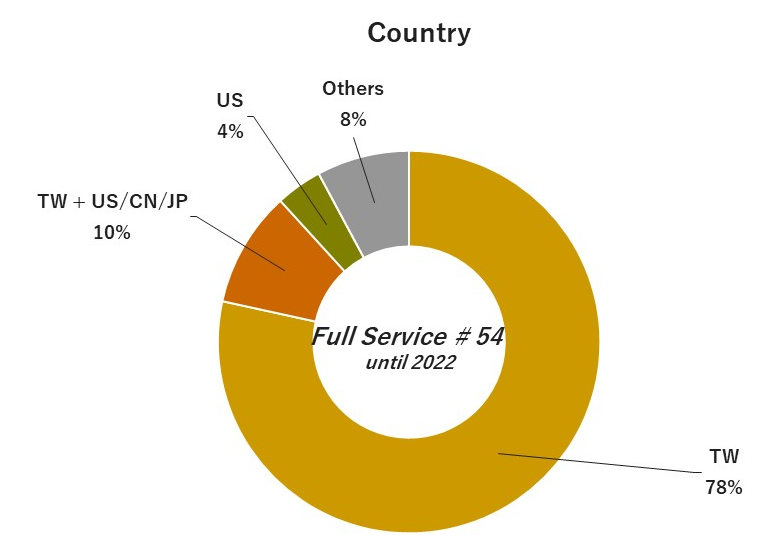 |
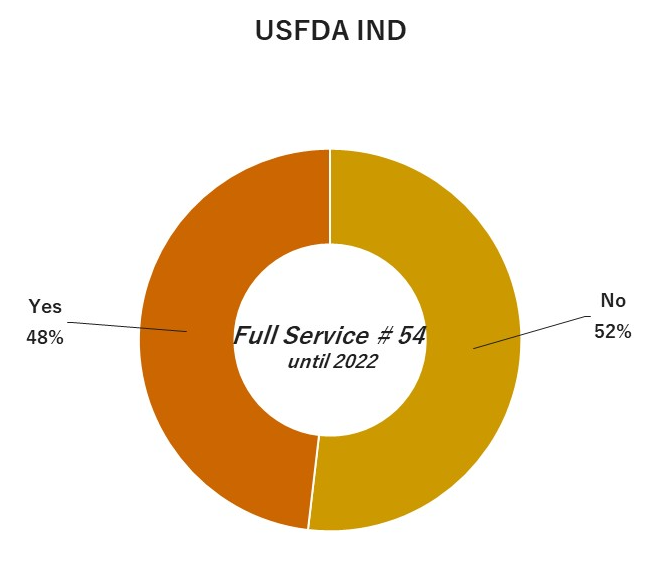 |